Abstrakt
Obezita a diabetes mellitus (diabezita) predstavujú významné rizikové faktory zhubných nádorov. Prevencia a liečba obezity a diabetu je preto zároveň aj súčasťou prevencie nádorových chorôb. Farmakologická liečba diabetu môže viesť k zvýšenému alebo k zníženému riziku zhubných nádorov. Nádorové choroby sa spájajú s vysokým rizikom malnutrície a sarkopénie. Proteínovo-energetická malnutrícia môže v niektorých prípadoch progredovať až do kachexie. Včasná nutričná terapia onkologických pacientov dokáže nielen zabrániť nádorovej kachexii alebo ju aspoň oddialiť, ale tiež umožňuje zvýšiť toleranciu protinádorovej liečby. Onkologickým pacientom s diabetom možno pri indikácii klinickej výživy orálnymi nutričnými suplementmi (sipping) odporučiť kombináciu prípravkov špecifických pre diabetes spolu s prípravkami určenými pre onkologických pacientov obohatenými o omega-3 mastné kyseliny. V prípade používania výlučne diabeticky špecifických prípravkov, ktoré omega-3 MK neobsahujú, možno esenciálne omega-3 MK z rybieho tuku (EPA, DHA) s imunomodulačným účinkom podávať vo forme výživových doplnkov.
Kľúčové slová: obezita, diabetes mellitus, zhubný nádor, onkologický pacient, orálne nutričné suplementy, ONS, nutričné formuly špecifické pre diabetes, NFŠD
Diabetes mellitus ako rizikový faktor zhubných nádorov
Doterajšie výskumy potvrdili zvýšenú incidenciu zhubných nádorov (ZN) u pacientov s diabetes mellitus (DM) 1. i 2. typu. Diabetes mellitus patrí medzi rizikové faktory viacerých druhov nádorov, a to predovšetkým kolorektálneho karcinómu a ďalších tumorov gastrointestinálneho traktu (GIT), hepatocelulárneho karcinómu, karcinómu pankreasu a u žien takisto aj karcinómov prsníka, ovárií a endometria. Súhrnná analýza početných metaanalýz a kohortných štúdií okrem vyššie uvedených nádorov zistila aj rizikový vplyv DM vo vzťahu ku karcinómu žlčových ciest (intrahepatálny cholangiokarcinóm), prostaty, obličiek a štítnej žľazy.(1, 2) Navyše existujú dôkazy aj o tom, že DM nezvyšuje len riziko ZN, ale takisto zvyšuje aj ich mortalitu. Ďalšie známe rizikové faktory onkologických chorôb, akými je vek, obezita, pohybová inaktivita a sedavý životný štýl alebo fajčenie, prispievajú svojím podielom k zvýšenému nádorovému riziku u diabetických pacientov. Medzi biologické mechanizmy, pomocou ktorých DM podporuje výskyt ZN, patrí hyperglykémia, hyperinzulínémia, zvýšená bioaktivita inzulínového rastového faktora (Insulin-like Growth Factor 1, IGF 1), oxidačný stres, dysregulácia pohlavných hormónov a chronický subklinický zápal (ktorý je prítomný aj v prediabetickej fáze viscerálnej obezity). Zatiaľ neexistujú ešte definitívne vedecké dôkazy o účinnom znižovaní nádorových rizík špecifických druhov rakoviny užívaním antidiabetickej medikácie. V rámci prevencie nádorových ochorení má preto veľký význam primárna prevencia obezity a diabetu (DM 2. typu). Navyše, pacienti, ktorí už majú DM, by mali v súlade so svojím vekom a pohlavím v záujme zvýšenia šancí včasnej diagnostiky nádorov podstupovať cielené skríningové vyšetrenia.(3) V prípade DM 2. typu sa zistilo vyššie riziko rakoviny ako v prípade DM 1. typu. Aj keď samotná hyperglykémia má významný vplyv na nádorové procesy, zdá sa, že aj ďalšie faktory, ktoré súvisia s obezitou a ostatnými metabolickými abnormalitami, sú nevyhnutné na zvyšovanie nádorového rizika, pričom tieto faktory nie sú typické pre DM 1. typu. Viaceré štúdie pri sledovaní celkovej nádorovej mortality potvrdili vyššiu úmrtnosť na nádorové ochorenie v tých prípadoch, keď išlo o diabetikov.(4) Keďže obezita je najdôležitejším faktorom pre rozvoj DM 2. typu, nie je prekvapujúce, že väčšina nádorov spojených s obezitou sa tiež asociuje s DM 2. typu.(5) Vzájomné korelácie však nie sú identické. Obezita aj diabetes prispievajú k rakovine nezávisle, pričom ich vplyv môže byť zároveň aditívny alebo synergický.(6)
Liečba diabetu a jej vplyv na zhubné nádory
Diabetogénny vplyv onkologickej liečby
Dôkazy z viacerých observačných i experimentálnych štúdií zatiaľ iba naznačujú možnosť, že niektoré lieky, ktoré sa používajú na liečbu diabetu, môžu viesť k zvýšenému alebo zníženému riziku zhubných nádorov. Ukázalo sa, že antidiabetická terapia sulfonylureou a exogénnym podávaním inzulínu sa asociujú s hyperinzulinémiou a zvyšujú nádorové riziko, zatiaľ čo liečba metformínom sa spája so zlepšením inzulínovej rezistencie a riziko zhubných nádorov môže znižovať. Vo všeobecnosti však možno konštatovať, že v súčasnom období ešte neexistujú definitívne dôkazy o karcinogénnom účinku akýchkoľvek antidiabetických liekov.(7, 8) Na druhej strane sú známe aj prípady, keď cielená onkologická liečba môže viesť k nežiaducemu dočasnému alebo aj trvalému diabetu. Príkladom môže byť podávanie kortikosteroidov vo vysokých dávkach, cisplatiny, tyrozínkinázy alebo pyrimidínového analógu 5-fluorouracil. Diabetogénny efekt môže byť dôsledkom rozvoja hyperglykémie alebo inzulínovej rezistencie.(5)
Osobitý prístup k problematike výživy a podpornej nutričnej terapie onkologických pacientov
Nádorové ochorenia spolu so srdcovo-cievnymi chorobami patria medzi hlavné príčiny chorobnosti a úmrtnosti na celom svete. Očakáva sa, že výskyt onkologických chorôb bude v nasledujúcich desaťročiach naďalej stúpať. Mnohí onkologickí pacienti majú v priebehu svojho ochorenia nedostatočný stav výživy (malnutrícia), pričom najčastejšie ide o proteínovo-energetickú malnutríciu. Malnutrícia sa pozoruje v 40 – 80 % onkologických pacientov, a dokonca až v 80 – 90 % pacientov v pokročilom štádiu nádorového ochorenia. Malnutrícia má negatívny vplyv na toleranciu protinádorovej liečby a celkový priebeh a klinický stav choroby. Malnutrícia viazaná na nádorové ochorenie je výsledkom viacerých, pre zhubné nádory špecifických faktorov a okolností. Okrem zníženého príjmu stravy (energie a nutrientov) v dôsledku anorexie a narušeného vnímania chuti významne prispieva k nádorovej malnutrícii aj hypermetabolizmus a zvýšený výdaj energie spôsobený systémovou inflamáciou, ktorá vedie k zvýšenému katabolizmu a zmenám v metabolizme proteínov (zvýšený obrat) a sacharidov (inzulínová rezistencia a znížená tolerancia glukózy). Výsledkom takéhoto stavu je významný pokles telesnej hmotnosti s následnými zmenami telesného zloženia (úbytok kostrového svalstva i telesného tuku), ako aj poklesom fyzických funkcií a kondície. Pri progresívnej nekontrolovateľnej strate hmotnosti, svalovej i tukovej hmoty dochádza postupne k nádorovej kachexii, ktorá sa pokladá za pokročilé štádium malnutrície, vyznačujúce sa kontinuálnym úpadkom celkového stavu pacienta, ktoré už nemožno zvrátiť bežnou stravou a konvenčnou nutričnou starostlivosťou, čiže bez použitia orálnych nutričných suplementov (ONS). Jedným zo základných prejavov nádorovej malnutrície je progresívny úbytok a vyčerpanie kostrového svalstva (sarkopénia), ktorý sa prejavuje poklesom svalovej sily a zhoršenou kvalitou života. K sarkopénii môže dôjsť v ktorejkoľvek fáze nádorového ochorenia, či už v kuratívnej, alebo paliatívnej. Sarkopénia sa pritom môže vyskytovať aj u onkologických pacientov s obezitou a vyznačuje sa nedostatkom beztukovej hmoty u obéznych jedincov (obrázok č. 1).(9, 10) Prítomnosť sarkopenickej obezity je obzvlášť rizikovým prediktorom nepriaznivého priebehu a zlej prognózy u onkologických pacientov. Podľa nového európskeho konsenzu a definícií nie je sarkopénia viazaná výlučne na staršie osoby (seniorov), ale môže sa začať rozvíjať už v podstatne mladšom veku. Pokladá sa za svalovú chorobu, v popredí ktorej je okrem úbytku svalovej hmoty aj pokles svalovej sily. Vyznačuje sa poklesom nielen kvantity, ale aj kvality svalovej hmoty.(11)
Cieľom nutričnej terapie a metabolických intervencií onkologických pacientov je zlepšiť príjem energie, bielkovín a ostatných nutrientov, zmierniť metabolické poruchy, ku ktorým dochádza v dôsledku zhubného nádoru, a udržať kostrové svalstvo a fyzickú kondíciu v čo najlepšej forme. V neposlednom rade môže včasná a správne aplikovaná nutričná terapia znížiť riziko predčasného ukončenia alebo prerušenia cielenej protinádorovej liečby v dôsledku jej zníženej tolerancie a zlepšiť celkovú kvalitu života.
Súčasťou komplexnej nutričnej intervencie onkologických pacientov zameranej na prevenciu a liečbu malnutrície sú:(12)
• Nutričné poradenstvo: ide o cielenú a profesionálnu komunikáciu s onkologickými pacientmi a prvú líniu nutričnej terapie zameranej na edukáciu o účelných zmenách v stravovacích návykoch onkologických pacientov.
• Orálne nutričné suplementy (ONS): komerčne vyrábané, väčšinou kompletné nutričné zmesi určené na orálnu konzumáciu (sipping) sa často predpisujú ako doplnková výživa k príjmu stravy.
• Enterálna a parenterálna výživa: pri nemožnosti dosiahnuť požadovaný príjem energie a nutrientov pomocou nutričného poradenstva a podpornou výživou prípravkami ONS sa indikuje doplnková alebo kompletná enterálna a v prípade nevyhnutnosti aj parenterálna výživa.
• Fyzikálna terapia a pohybová aktivita: podpora telesných aktivít, ktoré sú súčasťou každodenného života, ako aj aeróbne a odporové cvičenia zamerané na udržiavanie kostrových svalov a svalovej sily by mali byť rutinnou súčasťou komplexnej terapie onkologických pacientov. Prostriedky fyzikálnej liečby podporujú retenciu a utilizáciu nutrientov a posilňujú anabolické procesy pacientov.
• Farmakoterapia: u ťažko malnutričných pacientov v pokročilom štádiu nádorovej choroby sú indikované farmaká, ktoré môžu zvýšiť chuť do jedla, podporiť črevnú motilitu, znížiť úroveň systémovej inflamácie a hyperkatabolizmu a podporiť svalovú hmotu a anabolické reakcie v organizme.
Nutričná liečba onkologických pacientov má svoje špecifiká a bola predmetom mnohých publikácií vo svetovej i domácej literatúre. Osobitný význam majú najmä oficiálne výživové odporúčania pre onkologických pacientov Európskej spoločnosti parenterálnej a enterálnej výživy (European Society for Parenteral and Enteral Nutrition, ESPEN) – pozrite citácie č. 10 a 12. Osobitostiam nutričnej starostlivosti o onkologických pacientov sa venovalo aj niekoľko prehľadových článkov v predchádzajúcich číslach časopisu NUTRITION NEWS (napríklad: Tomáš, M., Pinďák, D. ESPEN – Odporúčania pre onkológiu – 2017, 1. časť. Praktické odporúčania pre klinickú prax/september 2017; Paulová, P. Špecifiká vo výžive onkologických pacientov/máj 2019; ako aj ďalšie články). Čitateľov so záujmom o danú problematiku preto odkazujeme aj na tieto, ako aj na ďalšie podobné publikácie.
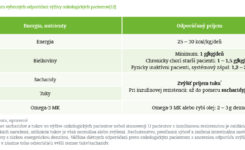
Výber nutričnej podpory a starostlivosti závisí od celkového stavu výživy pacienta, jeho chuti do jedla, ako aj od konkrétneho typu a štádia zhubného nádoru. Odporúča sa skríning nutričného stavu pacientov vo včasných fázach onkologickej liečby, ktorého súčasťou má byť aj pátranie po anorexii, ako aj po existujúcej alebo hroziacej malnutrícii a sarkopénii, a to s využitím dostupných antropometrických metód, bioelektrickej impedančnej analýzy a laboratórnych vyšetrení biomarkerov zameraných na detekciu systémovej inflamácie (napríklad C-reaktívny proteín, CRP) alebo zníženej výživy (napríklad albumín). Po stanovení celkovej potreby príjmu energie a základných živín (bielkoviny, sacharidy, tuky) sa pristupuje k tvorbe individuálneho nutričného plánu, pričom základný dôraz sa kladie na dostatočný príjem energie: 25 – 30 kcal/kg telesnej hmotnosti/deň a na príjem bielkovín: 1,2 – 1,5 g/kg telesnej hmotnosti/deň. V individuálnych prípadoch, napríklad pri rapídnom poklese telesnej hmotnosti a úbytku kostrového svalstva, závažných prejavoch systémového zápalu alebo u telesne inaktívnych, prípadne starších pacientov, môže byť potreba príjmu energie a bielkovín aj vyššia: energia: 35 kcal/kg/deň, bielkoviny: do 2 g/kg/deň.
Systémový zápal u onkologických pacientov inhibuje utilizáciu živín, podporuje katabolizmus a progresívny úbytok svalovej hmoty. Bežná strava obohatená o energiu a bielkoviny, podobne ako štandardné ONS, neznižuje systematickú inflamáciu, preto najnovšie aktualizované nutričné stratégie odporúčajú v rámci výživy onkologických pacientov podporovať chuť do jedla, anabolizmus, celkovú hmotnosť aj beztukovú, a predovšetkým svalovú hmotu pomocou látok, ktoré majú antikatabolické, antiinflamatórne a imunomodulačné vlastnosti. Do úvahy prichádzajú esenciálne aminokyseliny s rozvetveným reťazcom (leucín, izoleucín, valín, arginín) a esenciálne viacnenasýtené omega-3 mastné kyseliny (MK) s dlhým reťazcom (podanie 2 – 3 g rybieho tuku alebo omega-3 MK denne). Dobrú službu urobí aj celkový zvýšený príjem tukov (30 % z celkového denného energetického príjmu, výnimočne i viac až do 40 %) s využitím MK so stredne dlhým reťazcom (Medium Chain Fatty Acids, MCFA) pre ich lepšiu toleranciu pri malabsorpcii tukov (nevyžadujú prítomnosť solí žlčových kyselín) (tabuľka č. 1).
Špecifiká výživy onkologicky chorých diabetikov
Dobrá kontrola glykémií u pacientov s DM 1 aj DM 2 má rozhodujúci vplyv na dlhodobé klinické dôsledky diabetu. Naopak, hyperglykémia môže mať za následok komplikácie a komorbidity ohrozujúce život diabetom postihnutých jedincov. Navyše sa ukazuje, že viacero závažných chorôb – či už sú to úrazy, mozgový iktus, alebo iné kritické stavy – má horší priebeh i prognózu, pokiaľ je prítomná hyperglykémia.(13) Pre pacientov so zníženou toleranciou glukózy a s diabetom sú v prípade malnutrície a potreby podávať ONS určené nutričné formuly špecifické pre diabetikov (NFŠD). Sú to prípravky, ktorých osobitné nutričné zloženie umožňuje dosiahnuť nižšiu postprandiálnu glykémiu u pacientov s DM 1, ako aj u obéznych pacientov s DM 2. Tento účinok dosahujú prostredníctvom priamej stimulácie sekrécie inzulínu z β buniek pankreasu alebo nepriamo stimuláciou produkcie GLP-1 (glucagon-like peptide-1).(14) NFŠD obsahujú definované nutričné zloženie, ktoré pôsobí priaznivo na lepšiu glykemickú kontrolu (vláknina, mononenasýtené MK, sójový proteín, antioxidanty).
V starších aj novších prácach mnohí autori potvrdili priaznivé účinky viacerých nutrientov na kontrolu glykémie. Systematický prehľad výsledkov 19 randomizovaných kontrolných štúdií (RCT) poukázal na fakt, že krátkodobé i dlhodobé používanie NFŠD, či už vo forme orálnych suplementov, alebo sondovej výživy, sa asociuje s lepšou kontrolou glykémie v porovnaní so štandardnými formulami. Dlhodobá nutričná podpora NFŠD dokáže u diabetikov redukovať výskyt chronických diabetických komplikácií vrátane srdcovo-cievnych chorôb.(13) Japonskí autori na vzorke 4 339 pacientov s DM 2 potvrdili, že zvýšený príjem rastlinnej vlákniny u pacientov s DM 2 sa spája s lepšou kontrolou glykémie a navyše znižuje účinok rizikových faktorov kardiovaskulárnych (napríklad hypertenzia, metabolický syndróm, mikroinflamácia), ako aj chronických obličkových chorôb.(15) Ďalšia metaanalýza analyzovala 60 RCT so zaradením 605 pacientov, pričom sa takisto sledoval vplyv vlákniny na kontrolu glykémií u pacientov s DM 2. Výsledky potvrdili, že strava bohatá na vlákninu (v niektorých štúdiách až 42,5 g/deň) alebo užívanie výživových doplnkov s obsahom rozpustnej vlákniny (až do 15 g/deň) dokázala znížiť absolútne hodnoty glykovaného hemoglobínu o 0,55 % a glykémie nalačno o 9,97 mg/dl (0,5 mmol/l). Autori konštatovali, že zvýšený príjem vlákniny zlepšuje kontrolu glykémií, a môže sa teda využiť ako adjuvantný prostriedok pri liečbe pacientov s DM 2.(16) Okrem toho, že strava s nízkym glykemickým indexom (GI) má priaznivý vplyv na kontrolu glykémie u pacientov s DM, prináša aj metabolické benefity pre všeobecnú (zdravú) populáciu. Prototypom sacharidu s nízkym GI je prirodzene sa vyskytujúci disacharid – izomaltulóza, ktorá sa dá komerčne vyrobiť zo sacharózy (repného cukru). Izomaltulóza sa v súčasnosti používa ako alternatíva cukrov pri výrobe rôznych potravín a nápojov, ale pridáva sa aj do špeciálnych prípravkov používaných ako formulované diéty v klinickej výžive. Nemeckí autori vypracovali v roku 2017 prehľad klinických štúdií, ktoré sledovali účinky izomaltulózy na glykémiu, ako aj na oxidáciu lipidov, a porovnávali ich s účinkami bežných cukrov a sacharidov. Výsledky analytickej štúdie potvrdili, že diéty aj nápoje, ktoré mali nízky GI na podklade izomaltulózy, majú pri liečbe cukrovky priaznivé účinky na viacero sledovaných parametrov vrátane dosahovania lepších fyzických výkonov sledovaných pacientov počas cvičenia i po ňom. Tieto účinky izomaltulózy sú výhodné na využitie u pacientov s DM 2 vzhľadom na to, sa sa u nich s cieľom znižovania postprandiálnej hyperglykémie a kontroly glykémií odporúča strava s nízkym GI.(17) Aj u diabetických pacientov, ktorí trpia malnutríciou, treba pri liečebnej výžive myslieť na ochranu svalovej hmoty (kostrového svalstva) a udržanie svalovej sily. Vedeckými výskumami viacerých autorov sa zistilo, že účinok rôznych druhov bielkovín v potravinách na metabolizmus, a to predovšetkým na syntézu svalových proteínov, je odlišný. Ako príklad možno uviesť experimentálnu štúdiu holandských autorov z roku 2011, v ktorej na vzorke 48 starších mužov vo veku 73 – 75 rokov potvrdili, že srvátkové bielkoviny stimulujú u nich postprandiálnu tvorbu a akumuláciu svalových proteínov účinnejšie než kazeín alebo hydrolyzát kazeínu. Tento účinok sa pripisuje rýchlejšiemu tráveniu a vstrebávaniu srvátky a vyššiemu obsahu aminokyseliny leucín v srvátke oproti kazeínu. Potvrdilo sa teda, že bielkoviny srvátky podporujú syntézu svalových proteínov, čo možno s výhodou využiť v klinickej praxi a nutričných stratégiách pri malnutrícii spojenej s úbytkom svalovej hmoty a poklese svalových funkcií – napríklad u onkologických alebo diabetických pacientov s malnutríciou a sarkopéniou.(18) Vzhľadom na vedecky potvrdené účinky srvátkových proteínov na metabolizmus svalovej hmoty sa pridávajú do prípravkov vysokoenergetickej klinickej výživy, ktoré sú osobitne určené na nutričnú liečbu malnutričných pacientov so ZN a s DM. Recentná metaanalýza a systematický prehľad relevantných štúdií potvrdili, že NFŠD so zvýšeným obsahom mononenasýtených MK podávané vo forme ONS alebo sondovej výživy môžu v porovnaní so štandardnými ONS zlepšiť kontrolu glykémií a znížiť metabolické riziká u pacientov s DM, ako aj pri stresom indukovanej hyperglykémii.(19)
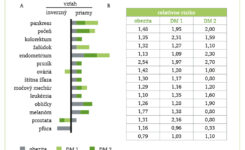
Medzi onkologickými pacientmi tvoria diabetici vysoký podiel. V USA trpí každý 10. dospelý občan DM, pričom DM 2 z toho tvorí približne 90 – 95 % prípadov. V európskom regióne žije približne 60 miliónov diabetikov, čo predstavuje približne 10,3 % mužov a 9,6 % žien vo veku nad 25 rokov. Prevalencia DM sa v európskom regióne zvyšuje vo všetkých vekových skupinách. V Slovenskej republike podľa Národného centra zdravotníckych informácií (NCZI) bolo v roku 2017 evidovaných 354 726 diabetikov (165 285 mužov a 189 441 žien), čo predstavuje 6 517 prípadov na 100 000 obyvateľov. DM 2 patrí medzi najčastejšie príčiny nádorovej mortality (kolón, prsník po menopauze, pankreas, pečeň, obličky, endometrium, non-Hodgkinov lymfóm a pravdepodobne aj ďalšie ZN). Najdramatickejšie zvyšuje DM 2 riziko karcinómu pečene (+ 250 %), karcinómu pankreasu (+ 73 %) a karcinómu endometria (+ 60 – 100 %), ďalej karcinómu močového mechúra (+ 43 %), non-Hodgkinovho lymfómu (+ 41 %), kolorekta (+ 29 %) a prsníka po menopauze (+ 20 %). Mortalita na ZN je u diabetikov o 40 – 50 % vyššia než u onkologických pacientov bez diabetu. Zatiaľ ostáva nie plne objasnenou záležitosťou, či diabetes spôsobuje zvýšenú agresivitu ZN (napríklad prostredníctvom hyperglykémie alebo hyperinzulinémie), alebo či zdravotné problémy, ktoré sprevádzajú DM, zhoršujú odpoveď organizmu pacientov na protinádorovú terapiu, prípadne či sa uplatňujúli obe skupiny okolností.(20, 21)
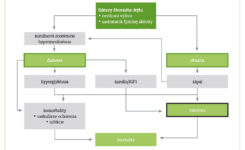
Nasledujúce GRAFY poukazujú na epidemiologickú súvislosť medzi obezitou, DM a ZN, ako aj na patologické mechanizmy, pomocou ktorých obezita a diabetes zvyšujú riziko nádorových chorôb.
Špecifiká výživy onkologického pacienta s diabetes mellitus a malnutríciou. Častou prítomnosťou diabetu u onkologických pacientov sa dostáva do popredia aj otázka ich výživy, či je to už pri obezite, alebo, naopak, pri hroziacej alebo progredujúcej malnutrícii.
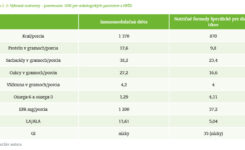
Nutričné formuly špecifické pre diabetes (NFŠD). Pre pacientov s diabetom a hyperglykémiou, ktorí pre malnutríciu vyžadujú podávanie ONS, sú indikované prípravky na pomalé popíjanie (sipping) s nízkym GI, tzv. nutričné formuly špecifické pre diabetes (NFŠD). Prípravky obsahujú kompletnú zostavu základných nutrientov, a radia sa tak do skupiny nutrične kompletnej výživy. Vďaka tomu, že obsahujú zmes rozpustnej a nerozpustnej vlákniny, pomaly stráviteľné škroby (rezistentný škrob) a špeciálne alternatívy cukrov (izomaltulóza), majú nízky glykemický index, v dôsledku čoho dokážu u diabetikov účinne podporovať kontrolu glykémie. Okrem špeciálneho zloženia sacharidov obsahuje receptúra aj účelné úpravy v obsahu bielkovín. Lepší metabolický vplyv na proteíny kostrového svalstva majú bielkoviny zo srvátky a sóje, preto v záujme prevencie a podpornej nutričnej liečby sarkopénie sa v NFŠD používajú srvátkové a sójové proteíny. Okrem vyššieho obsahu bielkovín majú prípravky aj vyšší obsah tukov s racionálnym zložením mastných kyselín. Pomer základných živín, ktorým sa podieľajú na celkovom obsahu energie, môže byť: bielkoviny 18,7 %, tuky 32,7 %, sacharidy bez vlákniny 44,8 % a vláknina 3,8 %. Prípravky v súlade s odporúčaniami ESPEN obsahujú vhodný mix vitamínov a minerálnych látok. Okrem pacientov s DM 1 a DM 2 sú tieto prípravky vhodné aj pre onkologických pacientov s cukrovkou.
Nutričné formuly určené pre pacientov s nádorovými chorobami sú podobne ako NFŠD takisto prípravkami s kompletnou zostavou základných nutrientov. Oproti bežným ONS však majú špeciálne upravené zloženie. V záujme ochrany svalovej hmoty a udržiavania svalových funkcií (svalová sila) obsahujú srvátkovú bielkovinu. Pre zabezpečenie imunomodulačného účinku a zmiernenie nežiaducich účinkov protinádorovej liečby (chemoterapia, rádioterapia) sú obohatené o esenciálne omega-3 mastné kyseliny z rybieho oleja (eikozapentaénová kyselina/EPA, dokozahexaénová kyselina/DHA). Pre dosiahnutie nízkeho glykemického účinku obsahujú podobne ako NFŠ zmes rozpustnej a nerozpustnej vlákniny. Vláknina navyše podporuje rast a množenie črevnej mikroflóry a pomáha udržiavať integritu črevnej bariéry a normálnu funkciu čriev. K nižšiemu GI prípravkov prispieva aj čiastočná náhrada bežných cukrov trehalózou, t. j. disacharidom zloženým z dvoch molekúl glukózy. Trehalóza sa v tenkom čreve štiepi enzýmom (trehaláza), ktorý sa nachádza na povrchu črevnej sliznice. Trehalóza je oproti bežnému cukru o niečo menej sladká (45 % sladivosť oproti sacharóze), ale dôležité je, že v porovnaní s glukózou alebo so sacharózou spôsobuje pomalší nárast postprandiálnej glykémie. Vďaka nízkemu GI i ostatným nutričným vlastnostiam sú prípravky určené pre pacientov s nádorovými chorobami vhodné aj pre onkologických pacientov, ktorí trpia zároveň na diabetes mellitus alebo inzulínovú rezistenciu spôsobenú či už samotným nádorom, alebo medikamentóznou liečbou.
Aj napriek tomu, že aktuálne nie sú ešte dostupné výsledky relevantných štúdií a chýbajú aj oficiálne medicínske odporúčania na podávanie ONS onkologickým pacientom s diabetes mellitus, je zrejmé, že pri indikácii klinickej výživy formou ONS (sipping) možno u pacientov so zhubnými nádormi a zároveň s diabetom použiť kombináciu prípravkov špecifických pre diabetes spolu s prípravkami určenými pre onkologických pacientov obohatenými o esenciálne omega-3 MK s dlhým reťazcom. V prípade používania výlučne diabeticky špecifických prípravkov, ktoré nie sú fortifikované o esenciálne omega-3 MK, možno tieto MK z rybieho tuku (EPA, DHA) s imunomodulačným účinkom podávať vo forme výživových doplnkov, a to v dávke 2 – 3 g denne (tabuľka č. 2).
Záver
Diabetes mellitus patrí spolu s obezitou medzi významné rizikové faktory viacerých zhubných nádorov. Prevencia a liečba obezity a diabetu je súčasťou prevencie nádorových chorôb. Nádorové choroby sa spájajú s vysokým rizikom malnutrície a sarkopénie. Proteínovo-energetická malnutrícia môže v niektorých prípadoch progredovať až do kachexie. Včasná nutričná terapia onkologických pacientov dokáže zabrániť alebo oddialiť rozvoj nádorovej kachexie a zároveň zvýšiť toleranciu protinádorovej liečby. Onkologickým pacientom s diabetom možno pri indikácii klinickej výživy orálnymi nutričnými suplementmi odporučiť kombináciu prípravkov špecifických pre diabetes spolu s prípravkami určenými pre onkologických pacientov obohatenými o omega-3 mastné kyseliny. Pokiaľ sa u týchto pacientov používajú len prípravky určené pre diabetikov, môžu sa im imunomodulačne pôsobiace omega-3 MK z rybieho oleja podávať vo forme výživových doplnkov.
doc. MUDr. Peter Minárik, PhD., MSc.
Onkologický ústav sv. Alžbety
E-mail: peterminarik57@gmail.com