Úvod
Cystická fibróza je monogenně, autozomálně recesivně dědičné multisystémové onemocnění charakterizované poruchou funkce transmembránového regulátoru vodivosti CFTR, s dominantními klinickými projevy v oblasti respiračního a gastrointestinálního traktu. Porucha funkce exokrinních žláz se uplatňuje již velmi časně, 85 % pacientů má pankreatickou insuficienci. U nich se potíže mohou rozvinout záhy po narození. Mekoniový ileus je obávanou perinatální komplikací cystické fibrózy.
V prvních letech života u většiny neléčených pacientů s cystickou fibrózou dominují projevy protein energetické malnutrice a karence vitaminů rozpustných v tucích. Zavedení substituce pankreatických enzymů a principů vysokokalorické a vysokoproteinové diety (160–180 % normálního kalorického příjmu) vedlo k výraznému zlepšení kvality života nemocných i prognózy onemocnění. Vedlo to k dominanci respiračních komplikací limitujících délku života pacientů, a to platí i v současnosti. V klinických studiích bylo opakovaně prokázáno, že pro výživový stav a kardiorespirační kondici pacienta platí reciproční, přímo úměrný vztah. Zavedení léčby CFTR modulátory v novém tisíciletí poskytuje pacientům s cystickou fibrózou zásadní zlepšení kvality života, otevírá jim nové životní perspektivy. Kauzálním vlivem na poruchu CFTR kanálu dochází k ovlivnění patogeneze nemoci na mnoha úrovních. Zásadně se mění i přístup k nutriční podpoře pacientů.
Patogeneze malnutrice u cystické fibrózy, vliv modulátorové léčby
Komplexní změny vedoucí k malnutrici u cystické fibrózy zahrnují primárně následky postižení funkce exokrinního pankreatu, jater, žlučových cest, ale i drobných sekrečních žláz tenkého střeva. Malnutrice lipidů je všeobecně známa, nicméně porucha trávení a vstřebávání se týká prakticky všech složek potravy. Ke klinickým projevům postižení trávicího traktu zásadně přispívá i střevní dysmikrobie.
S prodloužením života pacienta s cystickou fibrózou a kumulací respiračních projevů dochází
k prohloubení negativity energetické bilance – k insuficienci na straně příjmu zdrojů dochází
i k patologickému zvýšení (ne jenom) energetického výdeje. Změny výživového stavu po zavedení léčby CFTR modulátory popisuje tabulka níže. Modulátorová léčba ovlivňuje patogenezi cystické fibrózy kauzálně na mnoha úrovních.
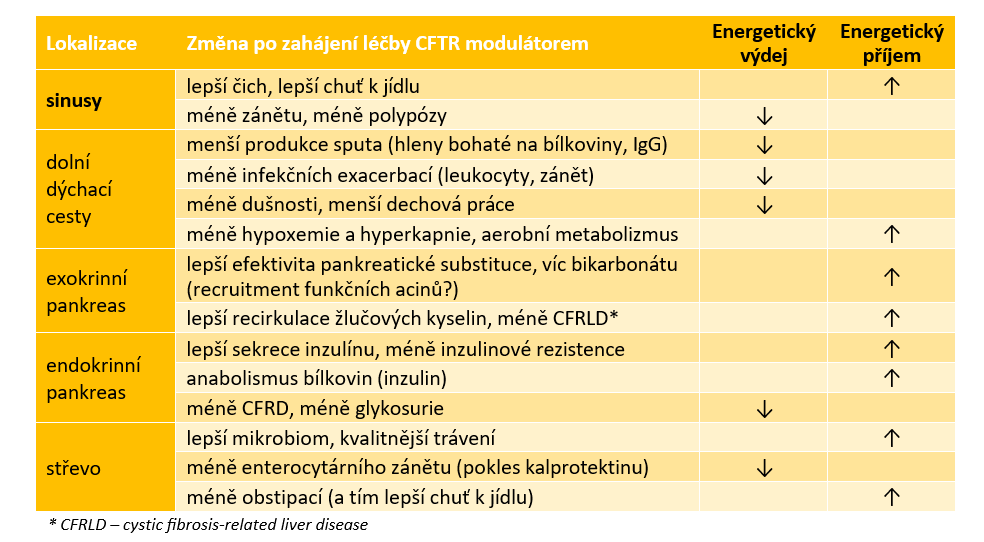
Kvantitativní a kvalitativní změny nutričního stavu
Růst dětí s cystickou fibrózou na modulátorové léčbě je příznivě ovlivněn změnou nutričního stavu
i sníženou frekvencí respiračních komplikací (studie ENVISION, GOAL). Jedním z biochemických ukazatelů je IGF-1, jehož hladina byla signifikantně vyšší (vliv růstového hormonu, inzulinu, kortikoidů). Předpokládá se intrinsický vliv CFTR na blízkou WNT signalizaci.
Hmotnost a BMI na léčbě CFTR modulátory signifikantně stoupá (studie ENVISION, STRIVE, VX17-445-103). BMI je primárně sledovaným ukazatelem nutričního stavu ve studiích s modulátory (spolu s FEV1), změny složení těla jsou méně často monitorovány. Korelace mezi FEV1 s FFM (fat-free mass) se ukazuje být silnější než s BMI. Ve studiích byla po zahájení léčby modulátory nejprve pozorována změna FFM (přesuny iontů na membránách), následně dochází ke vzestupu především FM (fat mass). Obezita se proto stává reálnou a již přítomnou hrozbou pro pacienty s cystickou fibrózou. V americkém registru cystické fibrózy (CF Foundation Patient Registry, CFFPR) je mezi lety 2000 a 2020 pozorován vzestup incidence nadváhy z 8 % na 17 %, obezity ze 2 % na 7 %. Současně je známo, že BMI nad 85. percentilem plicní funkce zhoršuje. Se stoupající incidencí obezity a prodloužením délky života se přímo nabízí otázka metabolického syndromu. Ve studii z USA z roku 2021 byl za necelého 1,5 roku (11/2019–03/2021) sledování prokázán signifikantní vzestup výskytu metabolického syndromu z 5 % na 16 % (p < 0,001). Výskyt civilizačních chorob se stává z tohoto pohledu i díky prodloužení dožití pacientů s cystickou fibrózou reálnou hrozbou.
Diabetes mellitus vázaný na cystickou fibrózu (cystic-fibrosis related diabetes, CFRD) je nepříznivou komplikací zkracující život především mladých dospělých žen s diagnózou cystické fibrózy. Léčba CFTR modulátory má jistý vliv i na výskyt CFRD. Ve švýcarské studii z roku 2022 byl příznivý posun v kategoriích prediabetu a diabetu prokázán ve skupině adolescentů s cystickou fibrózou. V dynamické studii byl popsán vliv na časnou postprandiální sekreci inzulinu (vyšší a časnější peak inzulinemie). Mechanismus účinku není přesně znám, předpokládá se přítomnost CFTR kanálu na β buňkách pankreatu, zvýšená sekrece inkretinů z enterocytů a lepší periferní inzulinová senzitivita při menším systémovém zánětu.
U mladého pacienta s cystickou fibrózou se zachovanou endokrinní funkcí se stává CFRD potenciálně preventabilní/oddálitelnou komplikací.
Vitaminy rozpustné v tucích jsou důležitým aspektem kvalitní výživy u pankreaticky insuficientních pacientů. Hladina vitaminu D se na modulátorové léčbě signifikantně zvyšuje (2021, p = 0,01). Tato změna je příznivá vzhledem ke známé korelaci mezi klinickým stavem pacienta a jeho aktuální hladinou vitaminu D (korelace s FEV1 i počtem exacerbací). Vitamin A při vzestupu hladiny může vést naopak
k nežádoucím projevům (edém papil, pseudotumor cerebri), hladinu je potřeba monitorovat obzvláště
u těhotných žen (teratogenní potenciál hypervitaminózy A).
Nové výživové doporučení
Se zavedením léčby CFTR modulátory se zásadně změnil přístup k nutriční podpoře pacienta s cystickou fibrózou. Univerzálně doporučenou vysokokalorickou a vysokoproteinovou výživu bylo potřebné modifikovat, nebo opustit. U pacientů na léčbě CFTR modulátory se dostává do popředí význam racionální, zdravé stravy. Vzhledem k těmto novinkám bylo vypracováno krátké cílené výživové doporučení ve formě brožurky pro naše pacienty.
Závěr
Nutriční doporučení pro pacienty s cystickou fibrózou je v současnosti nutné individualizovat. Vzhledem
k tomu, že i když většina našich pacientů dosáhne na nejmodernější léčbu CFTR modulátory, nemálo jich je (nejčastěji kvůli minoritním mutacím) nadále na symptomatické terapii. Výživové doporučení je proto nutné nastavit co nejlépe podle individuálních potřeb každého pacienta.
Seznam použité literatury
- Turck D, Braegger ChP, Colombo C, et al. ESPEN-ESPGHAN-ECFS guidelines on nutrition care for infants, children and adults with cystic fibrosis. Clin Nutr. 2016; 35(3): 557–577.
- Grammatikopoulou MG, Vassilakou T, Goulis DG, et Standards of Nutritional Care for Patients with Cystic Fibrosis: A Methodological Primer and AGREE II Analysis of Guidelines. Children (Basel). 2021; 8(12): 1180.
- Hollander FM, de Roos NM, Heijerman HGM. The optimal approach to nutrition and cystic fibrosis: latest evidence and recommendations. Curr Opin Pulm Med. 2017; 23(6): 556–561.
- van der Haak N, King SJ, Crowder T, et Highlights from the nutrition guidelines for cystic fibrosis in Australia and New Zealand. J Cyst Fibros. 2020; 19(1): 16–25.
- Nutrition Education Materials (NEMO) [online], team Queensland Government: Cystic Fibrosis and gene modulator therapy nutrition considerations (2021). Dostupné na https://www.health.qld.gov.au/nutrition/patients
- Christian F, Thierman A, Shirley E, et Sustained Glycemic Control With Ivacaftor in Cystic Fibrosis-Related Diabetes. J Investig Med High Impact Case Rep. 2019; 7: 2324709619842898.
- Misgault B, Chatron E, Reynaud Q, et Effect of one-year lumacaftor-ivacaftor treatment on glucose tolerance abnormalities in cystic fibrosis patients. J Cyst Fibros. 2020; 19(5): 712–716.
- Moheet A, Beisang D, Zhang L, et Lumacaftor/ivacaftor therapy fails to increase insulin secretion in F508del/F508del CF patients. J Cyst Fibros. 2021; 20(2): 333–338.
- Colombo C, Foppiani A, Bisogno A, et Lumacaftor/ivacaftor in cystic fibrosis: effects on glucose metabolism and insulin secretion. J Endocrinol Invest. 2021; 44(10): 2213–2218.
- Kessler L. Can lumacaftor-ivacaftor reverse glucose-tolerance abnormalities in cystic fibrosis? J Cyst Fibros. 2020; 19(4): 666.
- Korten I, Kieninger E, Krueger L, et al. Short-Term Effects of Elexacaftor/Tezacaftor/Ivacaftor Combination on Glucose Tolerance in Young People With Cystic Fibrosis-An Observational Pilot Study. Front Pediatr. 2022; 10: 852551.
- Strandvik B. Nutrition in Cystic Fibrosis-Some Notes on the Fat Recommendations. Nutrients. 2022; 14(4): 853.
- Stalvey MS, Pace J, Niknian M, et Growth in Prepubertal Children With Cystic Fibrosis Treated With Ivacaftor. Pediatrics. 2017; 139(2): e20162522.
- Davies JC, Cunningham S, Harris WT, et Safety, pharmacokinetics, and pharmacodynamics of ivacaftor in patients aged 2-5 years with cystic fibrosis and a CFTR gating mutation (KIWI): an open-label, single-arm study. Lancet Respir Med. 2016; 4(2): 107–115.
- Bass R, Brownell JN, Stallings VA. The Impact of Highly Effective CFTR Modulators on Growth and Nutrition Status. Nutrients. 2021; 13(9): 2907.
- Bailey J, Rozga M, McDonald CM, et Effect of CFTR Modulators on Anthropometric Parameters in Individuals with Cystic Fibrosis: An Evidence Analysis Center Systematic Review. J Acad Nutr Diet. 2021; 121(7): 1364–1378.e2.
- King SJ, Tierney AC, Edgeworth D, et al. Body composition and weight changes after ivacaftor treatment in adults with cystic fibrosis carrying the G551 D cystic fibrosis transmembrane conductance regulator mutation: A double-blind, placebo-controlled, randomized, crossover study with open-label extension. Nutrition. 2021: 85: 111124.
- Petersen MC, Begnel L, Wallendorf M, et al. Effect of elexacaftor-tezacaftor-ivacaftor on body weight and metabolic parameters in adults with cystic fibrosis. J Cyst Fibros. 2022; 21(2): 265–271.
- Restoration of exocrine pancreatic function in child with lumacaftor/ivacaftor therapy in cystic fibrosis. J Cyst Fibros. 2022; 21(2): 264.
- Bailey J, Krick S, Fontaine KR. The Changing Landscape of Nutrition in Cystic Fibrosis: The Emergence of Overweight and Obesity. Nutrients. 2022; 14(6): 1216.
- Szentpetery S, Fernandez GS, Schechter MS, et Obesity in Cystic fibrosis: prevalence, trends and associated factors data from the US cystic fibrosis foundation patient registry. J Cyst Fibros. 2022; 21(5): 777–783.
- Ratti G, Rueschhoff A, Reisch J, et al. Ratti, G. et al. (2021) ‘17: Development of metabolic syndrome in a single-center cohort after initiation of elexacaftor/tezacaftor/ivacaftor. J Cyst Fibr. 2021; 20(Suppl 1): 1S1–S128.
- Wisniewski BL, Aylward SA, Jordan CO, et al. Hypervitaminosis A with fulminant secondary intracranial hypertension following personalized medicine-based Elexacaftor/Tezacaftor/Ivacaftor initiation in a preadolescent with cystic fibrosis. J Cyst Fibros. 2022; 21(3): e217–e220.
- The Effects of Ivacaftor on Bone Density and Microarchitecture in Children and Adults with Cystic Fibrosis. J Clin Endocrinol Metab. 2021; 106(3): e1248–e1261.
- Kuffel H, Hoppe J, Meier M, et al. Improvement in fat-soluble vitamin levels following highly effective cftr modulator use in children with CF. J Cyst Fibr. 2021; 20: S105.
- Daley T, Hughan K, Rayas M, et Vitamin D deficiency and its treatment in cystic fibrosis. J Cyst Fibr. 2019; Suppl 2: S66–S73.
- Rovner AJ, Stallings VA, Schall JI, et Vitamin D insufficiency in children, adolescents, and young adults with cystic fibrosis despite routine oral supplementation. Am J Clin Nutr. 2007; 86(6): 1694–1699.
- Wani WA, Nazir M, Bhat JI, et Vitamin D status correlates with the markers of cystic fibrosis-related pulmonary disease. Pediatr Neonatol. 2019; 60(2): 210–215.
- Wright BA, Ketchen NK, Rasmussen LN, et al. Impact of elexacaftor/tezacaftor/ivacaftor on vitamin D absorption in cystic fibrosis patients. Pediatr Pulmonol. 2022; 57(3): 655–657.
- Scott JA, Maarsingh H, Holguin F, et al. Arginine Therapy for Lung Diseases. Front Pharmacol. 2021; 12: 627503.
- Wilschanski M, Peckham D. Nutritional and metabolic management for cystic fibrosis in a post-cystic fibrosis transmembrane conductance modulator era. Curr Opin Pulm Med. 2022; 28(6): 577–583.





